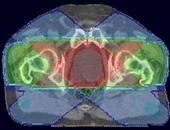
РАК ПИЩЕВОДА – ЛУЧЕВАЯ ТЕРАПИЯ
С момента открытия эффекта воздействия ионизирующих излучений подавляющего рост опухолевых тканей делались попытки использования их для лечения рака пищевода. В некоторых случаях удавалось достичь положительного эффекта в виде уменьшения болей, улучшения проходимости пищевода, а также увеличения продолжительности жизни у некоторых больных. Но только с развитием радиобиологии, физики ионизирующих излучений, дозиметрии, новых технических средств и источников излучения появилась возможность научно обосновать проведение лучевого лечения.
В настоящее время лучевое лечение широко применятся как для радикального так и для паллиативного лечения рака пищевода. Чаще всего используется гамма-излучение, тормозное излучение быстрые электроны.
Методы подведения излучения к патологическому очагу зависят от энергии излучения и аппаратуры, находящейся в распоряжении врача-радиолога.

Облучение может проводиться как дистанционно (через кожу), так и контактным методом (так называемая брахитерапия), когда источник излучения вводится прямо в просвет пищевода непосредственно к опухоли.
Применяются различные варианты дистанционного статического или подвижного облучения источниками излучений. Источники Сs137, Со60 используются также для внутриполостного облучения.
Задача облучения заключается в создании в заданном объеме средостения дозного максимума, имеющего форму кругового цилиндра диаметром 6-8 см длиной 18-20 см, в тех случаях, когда облучается весь пищевод. При этом дозный максимум должен включать всю опухоль, возможные участки внутристеночного метастазирования, а также околопищеводные зоны регионарных лимфатических узлов.
В тех случаях, когда поражены нижние отделы пищевода в объем облучения целесообразно включать паракардиальные зоны, малый сальник и зону левых желудочных лимфатических узлов.
Оптимальная поглощенная доза в очаге, при которой наблюдается полная резорбция опухоли пищевода, составляет 60-70Гр при облучении 5 раз в неделю и разовой очаговой дозе 1,5-2 Гр при классическом фракционировании дозы. При других вариантах фракционирования дозы, подводимые в течение дня, могут меняться, как могут меняться и разовые очаговые дозы.
При статическом облучении кожные поля располагаются по периметру грудной клетки, количество полей при гамма-облучении 34,1-2 - при использовании источников высоких энергий. При подвижном облучении ротация проводится в пределах 180-360 градусов.
Внутриполостное облучение осуществляется путем введения радиоактивных источников в просвет специального зонда, устанавливаемого в просвет пищевода в зоне расположения опухоли.
Положение носителя в пищеводе контролируется с помощью рентгенологического исследования. Чаще всего используется сочетание внутриполостного и наружного облучения. При этом достигается более оптимальное дозное распределение поглощенного излучения, чем при каждом из используемых вариантов облучения.
Сочетания внутриполостного и наружного облучения могут быть различными. Например, при достаточной ширине просвета пищевода сначала может использоваться внутриполостное облучение, а затем наружное. При выраженном стенозе пищевода лечение должно начаться с наружного облучения. Совместное использование дистанционной и контактной лучевой терапии носит название сочетанной лучевой терапии.
Необходимо отметить, что с повышением очаговой дозы наряду с повышением эффекта от лечения наблюдается увеличение частоты и тяжести осложнений.
Иногда в связи с выраженной дисфагией перед началом лучевой терапии приходится накладывать больному гастростому для питания. Кроме того во время операции возможно проведение качественной ревизии зон регионарного метастазирования ниже диафрагмы и, соответственно, появляется возможность обоснованно выбрать радикальное или паллиативное лечение. После эффективного завершения лечения гастростома может быть закрыта.
В последние годы все большее внимание онкологов привлекает возможность повышения эффективности лучевого лечения путем использования комбинации с использованием цитостатических препаратов и препаратов, увеличивающих чувствительность опухолевой ткани к облучению (радиосенсибилизаторов).
Использование цитостатических препаратов направлено, в основном, на возможность митотической синхронизации клеток опухоли и подведение дозы облучения в момент наибольшей уязвимости клеток. В качестве синхронизатора используется в последнее время 5-фторурацил, а в качестве радиосенсибилизатора - препараты платины.
Противопоказаниями к проведению лучевого лечения являются наличие перфорации опухоли и отдаленные метастазы в другие органы (в печень, почки, легкие).
Наличие множественных метастазов в шейно-надключичных, паракардиальных, левых желудочных и малом сальнике делает лучевое лечение в самостоятельном виде малоперспективным.
Наличие туберкулеза легких в активной форме также обычно служит противопоказанием к проведению лучевой терапии т. к. на фоне облучения быстро наступает генерализация или резкое обострение туберкулезного процесса.
Нарушения сердечной деятельности и функции почек, гипертоническая болезнь, острые воспалительные заболевания и изменения крови (лейкопения, анемия, лимфопения и т. д.) также ограничивают возможность проведения лучевого лечения.
Паллиативное лучевое лечение возможно у большинства больных раком пищевода, особенно оно показано после неудачной попытки хирургического лечения-пробной торакотомии.
Обезвоженных, истощенных и ослабленных больных необходимо специально готовить к лучевой терапии внутривенными инфузиями белковых препаратов, растворов электролитов, небольших количеств крови или ее компонентов. Хотя лечение таких больных редко бывает успешным.
Во время лучевого лечения больным назначают высококалорийную диету, богатую белками и витаминами. Пища должна быть теплой, полужидкой или жидкой консистенции и приниматься часто, мелкими порциями.
Отдаленные результаты лучевого лечения больных раком пищевода весьма далеки от оптимальных и ни в коей мере не могут считаться удовлетворительными.
Общий показатель 5 летней выживаемости колеблется от 3,5 до 8,5%. Даже использование разных вариантов фракционирования дозы позволило увеличить показатель пятилетней выживаемости при II стадии только до12,5±2,7%. Использование только тормозного излучения с В-протонами позволило получить показатель трехлетней выживаемости 15,5± 5,4%.
Остались вопросы? Напишите нам